| |
Como se señaló
en el esquema general sobre la función pulmonar con que
se inicia este libro, es posible diferenciar en el pulmón
tres compartimentos que tienen, a pesar de su estrecha integración,
fisonomías relativamente propias: las vías aéreas,
los espacios alveolares y el intersticio pulmonar (Figura
II). En este capítulo analizaremos las alteraciones
funcionales comunes y las específicas que se producen cuando
estas áreas son asiento de enfermedad. Este conocimiento
es básico para comprender, más adelante en los capítulos
de semiología, la génesis y el significado de diversos
síntomas y signos de enfermedades pulmonares, y para indicar
la aplicación del estudios funcionales respiratorios a
la solución de problemas clínicos.
ALTERACIONES FUNCIONALES POR COMPROMISO DE
LA VIA AEREA
La alteración funcional primaria más
importante que pueden originar las enfermedades de las vías
respiratorias, es la obstrucción al flujo aéreo.
Causas de obstrucción de la vía
aérea
El área de sección de la vía
aérea puede disminuir como consecuencia de diversos mecanismos
patológicos. En las vías aéreas centrales
(faringe, laringe y tráquea) estos mecanismos incluyen:
- inflamación
- neoplasias
- estenosis cicatricial
- hipotonía de los músculos faríngeos
durante el sueño
- cuerpo extraño
- parálisis de cuerdas vocales
- compresión extrínseca
En las vía aéreas periféricas
(bronquios y bronquíolos) los mecanismos de obstrucción
son:
- contracción del músculo liso
- edema e infiltración celular inflamatoria de la mucosa
- retención de secreciones
- neoplasias
- estenosis cicatricial
- cuerpo extraño
- disminución del soporte elástico de las vías
aéreas intrapulmonares (Figura 14-1)
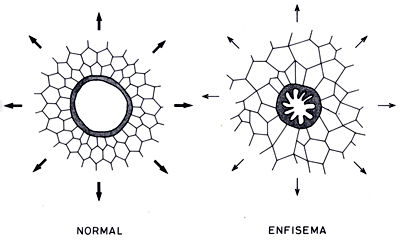
Figura 14-1. Disminución
de la tracción radial sobre la vía aérea
en el enfisema. En condiciones normales, el tejido elástico
del pulmón tracciona radialmente las vías
aéreas intraparenquimatosas, manteniendo abiertas
a aquellas que carecen de soporte cartilaginoso. En el
enfisema pulmonar hay una disminución de la tracción
radial debido a la destrucción de los tabiques
alveolares. Esto trae como consecuencia una disminución
del calibre de estas vías aéreas.
Por su configuración anatómica
y funcional, las consecuencias de la obstrucción de la
vía aérea central son muy diferentes a las de la
obstrucción de las vías aéreas periféricas.
Obstrucción de la vía aérea
central
Debido a su pequeña área de
sección, las vías centrales contribuyen en un elevado
porcentaje a la resistencia total de las vías aéreas
(RVA) (Tabla 2-2).Sin
embargo, el VEF1 solo se reduce cuando el diámetro
lumen traqueal cae por debajo de 8mm..
La
curva flujo volumen es, en
cambio mas sensible y sus características
varían según la localización intra o extratorácica
de la obstrucción. La presión que rodea la vía
aérea extratorácica (laringe y porción superior
de la tráquea) es la presión atmosférica,
que no varía durante la respiración. La presión
intraluminal se hace negativa durante la inspiración, por
lo que la vía aérea tiende a estrecharse en esta
fase. Durante la espiración, en cambio, la presión
intraluminal es positiva y la vía aérea se dilata
(Figura 14-2).
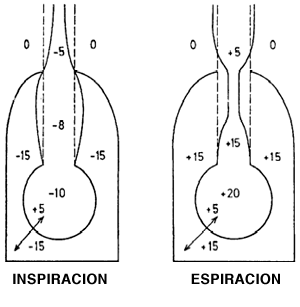
Figura 14-2. Cambios
del calibre de la vía aérea central durante
inspiración y espiración forzadas. La vía
aérea central extratorácica se estrecha
durante la inspiración y se dilata durante la espiración.
La vía aérea intratorácica, en cambio,
se dilata durante la inspiración y se estrecha
en espiración. Los cambios de calibre se acentúan
si existen lesiones obstructivas.
Por esta razón, las obstrucciones de la
vía extratorácica se manifiestan por un aumento
de la resistencia inspiratoria, mientras que la espiratoria puede
mantenerse normal.
El efecto de las obstrucciones de la porción
inferior de la tráquea, en cambio, depende de la relación
entre dos presiones que cambian durante la respiración:
la que existe dentro del conducto y la que existe dentro del tórax.
Aunque la presión intraluminal varía en el mismo
sentido que la presión extraluminal, normalmente se producen
diferencias debido al desgaste de presión producido por
la resistencia al flujo dentro de la vía aérea,
de manera que el calibre de la vía aérea intratorácica
se dilata durante la inspiración y se estrecha en espiración.
Cuando existe una obstrucción parcial de la vía
aérea central intratorácica el estrechamiento espiratorio
descrito la exagera, aumentando la resistencia espiratoria.
Para diferenciar entre la obstrucción
central y la periférica, resulta útil recurrir a
la curva flujo-volumen realizada en inspiración y espiración
forzadas. Como vimos en el capítulo 2, durante la espiración
forzada el flujo aéreo se limita por el colapso de la vía
aérea en los puntos de igual presión (PIP). Al comienzo
de la espiración, cuando el volumen pulmonar es alto, los
PIP se localizan en la tráquea y bronquios, con lo que
se exagera cualquier obstrucción existente en esas estructuras.
A medida que la espiración progresa y el volumen pulmonar
se va reduciendo, los PIP se desplazan hacia la periferia, exagerando
las obstrucciones localizadas en ese nivel.
La Figura 14-3 muestra las curvas flujo-volumen
obtenidas en un sujeto normal y en pacientes con obstrucción
de la vía aérea central. Además, se incluye
la curva de un paciente con obstrucción difusa de las vías
aéreas periféricas.

Figura 14-3. Curvas flujo-volumen
de un sujeto normal (A) y de pacientes con diferentes enfermedades
de la vía aérea. La curva B, de un paciente
con obstrucción de vía aérea central
(OVAC) extratorácica, muestra una meseta con disminución
de los flujos inspiratorios y conservación de los
flujos espiratorios. La curva C, de un paciente con OVAC
intratorácica, tiene una meseta con disminución
de los flujos espiratorios a volúmenes pulmonares
altos y flujos inspiratorios normales. La curva D, de un
paciente con OVAC fija, presenta disminución de los
flujos inspiratorios y espiratorios, con formación
de meseta. La curva E, de un paciente con obstrucción
bronquial difusa, muestra una disminución preponderante
de los flujos espiratorios a volúmenes pulmonares
bajos, sin formación de meseta.
En el sujeto normal (curva A), los flujos inspiratorios
y espiratorios máximos al 50% de CV son prácticamente
iguales. En la obstrucción central extratorácica
(curva B), existe una disminución marcada de los flujos
inspiratorios máximos con aplanamiento de la curva inspiratoria
y conservación de los flujos espiratorios. La curva C corresponde
a un paciente con obstrucción traqueal intratorácica:
se observa una disminución de los flujos espiratorios máximos
a volúmenes pulmonares altos, con indemnidad de los flujos
inspiratorios. Si la obstrucción traqueal está constituida
por un segmento rígido (obstrucción "fija"), la
zona estrechada no cambia notoriamente su diámetro interno
con los cambios de presión, por lo que la limitación
del flujo aéreo es similar en inspiración y espiración
(curva D). En este caso no es posible diferenciar la localización
intra o extratorácica de la lesión mediante la curva
flujo-volumen. La curva E fue obtenida en un paciente con obstrucción
bronquial periférica difusa. Se puede apreciar que existe
una disminución preponderante de los flujos espiratorios,
pero que, a diferencia de los pacientes con obstrucción
traqueal, esta disminución de flujos es más marcada
a volúmenes pulmonares bajos.
Si no se dispone de equipo para efectuar
una curva flujo-volumen, una información similar puede
obtenerse con la espirometría. Mediante este examen es
posible medir el volumen inspiratorio forzado del primer segundo
(VIF1), además del VEF1. En sujetos
normales la relación VEF1/VIF1 varía
entre 0,8 y 1,2. Valores superiores a este límite sugieren
obstrucción extratorácica. Los valores inferiores
a 0,8 pueden observarse tanto en obstrucción central intratorácica
como en obstrucción bronquial difusa. Una disminución
más acentuada del flujo máximo espiratorio (PEF)
que del VEF1 también sugiere obstrucción
traqueal intratorácica. Esto se debe a que el PEF representa
el flujo máximo logrado a volúmenes pulmonares altos,
mientras que el VEF1, incluye flujos espiratorios tanto
a volúmenes pulmonares altos como bajos.
Consecuencias funcionales
Los volúmenes y capacidades pulmonares
no se alteran significativamente en la obstrucción central,
salvo en trastornos extremos. La distensibilidad pulmonar es usualmente
normal. Tampoco se altera la relación  /Q,
ya que, estando las vías aéreas periféricas
normales, la distribución del aire inspirado y la perfusión
sanguínea no presentan alteraciones. En consecuencia, en
casos de obstrucción central corrientemente no existe hipoxemia.
En casos muy graves puede producirse fatiga muscular respiratoria
que lleva a hipoventilación alveolar con hipercapnia e
hipoxemia secundaria. /Q,
ya que, estando las vías aéreas periféricas
normales, la distribución del aire inspirado y la perfusión
sanguínea no presentan alteraciones. En consecuencia, en
casos de obstrucción central corrientemente no existe hipoxemia.
En casos muy graves puede producirse fatiga muscular respiratoria
que lleva a hipoventilación alveolar con hipercapnia e
hipoxemia secundaria.
Obstrucción de las vías aéreas
periféricas
Las consecuencias fisiológicas de
la obstrucción bronquial periférica difieren marcadamente
de acuerdo a su extensión, localización y grado.
Obstrucción localizada
En el caso de la obstrucción aislada
de una rama bronquial, los trastornos fisiológicos dependen
de su localización. La obstrucción de un bronquio
pequeño produce alteraciones fisiológicas mínimas,
que habitualmente no pueden detectarse en los exámenes
funcionales corrientes. En un bronquio mayor, como uno segmentario,
la obstrucción parcial puede producir alteraciones leves
en los gases arteriales (disminución de la relación /Q
con aumento de la PA-aO2), mientras que
la espirometría será probablemente normal. La obstrucción
completa de un bronquio mayor puede causar atelectasia del territorio
pulmonar correspondiente, con disminución del volumen pulmonar
detectable en la radiografía de tórax y alteraciones
funcionales de tipo restrictivo, que veremos más adelante.
Sin embargo, la obstrucción total de un bronquio mayor
no siempre produce colapso alveolar, debido a la existencia de
ventilación colateral a través de los poros de Kohn
que, en muchos casos, es suficiente para mantener insufladas las
zonas tributarias del bronquio ocluido. Las zonas ventiladas colateralmente
no se vacían durante una espiración máxima,
por lo que tienden a disminuir la CV y aumentar el VR. Debido
a la disminución del calibre bronquial en espiración,
ocasionalmente la obstrucción toma un carácter valvular,
permitiendo la entrada de aire en la inspiración e impidiendo
su salida en la espiración. Esto conduce a hiperinsuflación
del territorio comprometido, lo que limita la CV tanto por atrapamiento
de aire como por compresión de parénquima vecino. /Q
con aumento de la PA-aO2), mientras que
la espirometría será probablemente normal. La obstrucción
completa de un bronquio mayor puede causar atelectasia del territorio
pulmonar correspondiente, con disminución del volumen pulmonar
detectable en la radiografía de tórax y alteraciones
funcionales de tipo restrictivo, que veremos más adelante.
Sin embargo, la obstrucción total de un bronquio mayor
no siempre produce colapso alveolar, debido a la existencia de
ventilación colateral a través de los poros de Kohn
que, en muchos casos, es suficiente para mantener insufladas las
zonas tributarias del bronquio ocluido. Las zonas ventiladas colateralmente
no se vacían durante una espiración máxima,
por lo que tienden a disminuir la CV y aumentar el VR. Debido
a la disminución del calibre bronquial en espiración,
ocasionalmente la obstrucción toma un carácter valvular,
permitiendo la entrada de aire en la inspiración e impidiendo
su salida en la espiración. Esto conduce a hiperinsuflación
del territorio comprometido, lo que limita la CV tanto por atrapamiento
de aire como por compresión de parénquima vecino.
Obstrucción difusa: limitación
ventilatoria obstructiva
La obstrucción bronquial generalizada
es muy frecuente y se debe a noxas que actúan difusamente,
como el tabaco, o a la existencia de una hiperreactividad bronquial.
Esta última hace que la vía aérea responda
con obstrucción bronquial exagerada y extensa ante diferentes
estímulos irritantes o alérgicos. El trastorno funcional
producido en estas situaciones es característico y se denomina
limitación ventilatoria obstructiva.
La magnitud de las alteraciones funcionales depende
de la intensidad y extensión de la obstrucción de
bronquios y bronquíolos. Es necesario recordar que la contribución
de cada generación bronquial a la resistencia total de
la vía aérea disminuye marcadamente al alejarse
de la tráquea. Debido a este fenómeno, la obstrucción
de las vías aéreas pequeñas (menores de 2
mm de diámetro interno) viene a causar síntomas,
o se revela en la espirometría, en etapas relativamente
avanzadas. De la Tabla 2-2 puede
deducirse que un aumento del 100% en la resistencia de las vías
aéreas menores de 2 mm (equivalente a la obliteración
de la mitad de ellas) produce un aumento de sólo un 16%
en la resistencia total. Un trastorno de esa magnitud no produce
síntomas y no altera significativamente el VEF1.
Para detectar obstrucción de estas vías
se han diseñado múltiples pruebas funcionales, cuya
aplicación e interpretación son complejas, de manera
que se reservan básicamente para la investigación.
A medida que la obstrucción bronquial aumenta en intensidad,
el VEF1 disminuye progresivamente. Cuando esta caída
alcanza el límite inferior del valor teórico, se
puede afirmar con alta certeza que existe una disminución
clínicamente significativa de los flujos espiratorios máximos.
Un valor similar tiene una disminución del VEF1
más rápida que la que normalmente se produce con
la edad, aun cuando se mantenga dentro del rango normal.

Figura 14-4. Alteraciones
de los volúmenes pulmonares en los patrones obstructivo
y restrictivo. En el patrón obstructivo, la CPT está
normal o elevada a expensas del VR, ya que la CVF está
baja. La CRF está claramente aumentada, mientras que
el VEF1 y su relación con la CVF están disminuidos.
En el patrón restrictivo en cambio, existe una disminución
de CPT, CVF, CRF y VR. El VEF1 está disminuido proporcionalmente
a CVF, por lo que la relación VEF1 /CVF es normal.
Consecuencias funcionales
Volúmenes y capacidades.
La capacidad residual funcional está aumentada por diferentes
mecanismos.
a) Hiperinsuflación dinámica:
durante la
inspiración el aire entra con relativa facilidad porque la presión negativa y el aumento progresivo de volumen de los pulmonesdistiende los bronquiolos.En cambio como durante la espiración éstos colapsan
tempranamente, se produce un atrapamiento progresivo de aire.
Además, como el flujo aéreo está limitado,
el pulmón no alcanza a vaciarse totalmente en el tiempo
disponible antes de que se inicie la próxima inspiración
(Figura 14-4), lo que puede detectarse indirectamente por reducción
de la capacidad inspiratoria
b) Mantención del tono de los músculos
inspiratorios al final de la espiración, lo que mantiene
el pulmón más inflado, con aumento de la capacidad
residual funcional. Con ello se consigue que la tracción
elástica del pulmón mantenga los bronquios distendidos,
con disminución de su resistencia. Se trataría,
en consecuencia, de un fenómeno compensatorio del estrechamiento
bronquial.
c) Disminución de la retracción
elástica del pulmón, como sucede en el enfisema,
por destrucción de tabiques alveolares. La menor fuerza
de retracción del pulmón deja sin contrapeso a
la fuerza de expansión elástica del tórax,
con lo que el equilibrio entre ambas se establece a un mayor
volumen de reposo o capacidad residual funcional (Figuras
2-11 y 2-12).
La capacidad vital puede estar normal, pero
usualmente está disminuida en proporción al aumento
del volumen residual. La capacidad pulmonar total puede estar
normal o aumentada a expensas del
volumen residual. Por la misma razón la CI y el VRE suelen estar disminuidos. Cuando éste último cae a 500ml o menos la disnea se hace intolerable.
Volúmenes dinámicos. Son
los que más característicamente se alteran, por
el aumento de la resistencia en la vía aérea obstruida.
En el caso del enfisema se agrega el efecto de la disminución
de la retracción elástica del pulmón, que
es la fuerza propulsora del flujo aéreo espiratorio.
El VEF1 se encuentra disminuido
(Figura 14-4), tanto en su valor absoluto como en relación
con la capacidad vital del propio enfermo (VEF1/CVF
por debajo del límite inferior teórico).
El flujo máximo de media espiración
(FEF25-75) está muy disminuido y la ventilación
máxima voluntaria cae marcadamente, ya que depende básicamente
de los flujos aéreos que se logra alcanzar.
Mecánica ventilatoria
- La distensibilidad pulmonar medida en forma
estática puede estar normal, como sucede en casos de asma,
o aumentada, como se observa en enfisema.
- El trabajo respiratorio se encuentra aumentado
en proporción a la mayor resistencia de la vía aérea.
Además, debido a la hiperinsuflación pulmonar, el
volumen corriente se sitúa en la parte más horizontal
de la curva presión-volumen del pulmón (Figura
2-10), donde se necesita desarrollar mayor presión para
movilizar un volumen dado. - Además, existe un aumento
del trabajo de los músculos inspiratorios debido al fenómeno
denominado autoPEEP (de positive end expiratory pressure).
En condiciones normales, al final de la espiración la presión
alveolar es igual a la atmosférica. Si existe limitación
del flujo espiratorio por obstrucción bronquial, la presión
intraalveolar al final de la espiración sigue siendo algo
positiva, ya que el pulmón no alcanza a vaciarse antes
del inicio de la siguiente inspiración. Esto implica que
para hacer entrar aire a los alvéolos los músculos
inspiratorios deben ejercer un trabajo adicional, que es el necesario
para llevar la presión alveolar a cero y luego continuar
contrayéndose para crear la presión negativa necesaria
para hacer entrar el aire. Se ha calculado que éste es
el factor más importante en el aumento del trabajo de los
músculos inspiratorios en los pacientes con obstrucción
bronquial. Además, los musculos inspiratorios estan, en desventaja mecanica para contraerse porque se encuentran acortados debido la distensión del tórax
Ventilación alveolar
La ventilación alveolar no disminuye siempre
en proporción al grado de obstrucción bronquial
y aumento del trabajo respiratorio, debido a que existe una gran
variabilidad individual en el comportamiento de los centros respiratorios.
Esto se pone de manifiesto especialmente en obstrucciones crónicas
de grado avanzado: a igual compromiso funcional, un paciente puede
tener una PaCO2 normal y otro hipercapnia.
En el pasado, este fenómeno fue atribuido a diferencias
morfológicas en las lesiones del pulmón, pero actualmente
se acepta que el factor determinante es la sensibilidad de los
centros respiratorios, que tiene una base genética. En
algunos enfermos, con centros muy sensibles, la limitación
crónica del flujo aéreo conduciría a una
fuerte actividad compensatoria por efecto de estímulos
humorales y propioceptivos pulmonares. Esta mayor actividad alcanza
un grado tal como para mantener la ventilación alveolar
normal, aun a costa de un gran trabajo respiratorio, con la consiguiente
disnea o dificultad respiratoria subjetiva. En otros enfermos
los centros respiratorios se activarían menos, generándose
una una hipercapnia moderada , pero como no hay tanto aumento
del trabajo respiratorio hay menos disnea
Otro mecanismo que puede explicar la hipoventilación
crónica en estos pacientes, independientemente se las características
de sus centros respiratorios sería la fatiga crónica
de los músculos respiratorios. Estos músculos, al
contrario de los esqueléticos, no pueden detener su contracción
rítmica para descansar y sólo lo hacen durante la
espiración. En un individuo sano la respiración
en reposo demanda poco trabajo, por lo que el músculo es
capaz de recuperarse de episodios agudos de fatiga derivados de
mayor actividad física. En los enfermos obstructivos crónicos,
en cambio, el trabajo que exige la ventilación de reposo
está tan aumentado que probablemente no pueden recuperarse
de los episodios de fatiga aguda causados por pequeños
esfuerzos de la vida diaria o por infecciones, edema pulmonar,
etc. Con ello se crearía un estado crónico de fatiga
acumulada, por lo que los músculos no serían capaces
de responder a la mayor demanda de ventilación de los centros
respiratorios. Además, contribuyen a esta situación
otros factores, como la desventaja mecánica en que están
los músculos inspiratorios por el acortamiento que les
significa el tórax hiperinsuflado, la hipoxemia que afecta
a los músculos, la mala nutrición común en
estos enfermos, etc.
Intercambio gaseoso.
La obstrucción difusa conduce al aumento de áreas
alveolares con  /Q
bajo que se traducen por un aumento de la PA-aO2
que, al acentuarse, causa una caída progresiva de la PaO2.
Esta no logra ser superada por la limitada capacidad compensatoria
por la baja para el oxigeno que tienen las zonas restantes bien
ventiladas . En cambio, los efectos de las área con /Q
bajo que se traducen por un aumento de la PA-aO2
que, al acentuarse, causa una caída progresiva de la PaO2.
Esta no logra ser superada por la limitada capacidad compensatoria
por la baja para el oxigeno que tienen las zonas restantes bien
ventiladas . En cambio, los efectos de las área con  /Q
bajo sobre la PaCO2 pueden compensarse
eficazmente, hasta que la generalización de
unidades con /Q
bajo sobre la PaCO2 pueden compensarse
eficazmente, hasta que la generalización de
unidades con  /Q
bajo lleva a una hipoventilación alveolar global con hipercapnia. /Q
bajo lleva a una hipoventilación alveolar global con hipercapnia.
La difusión
de gases en la obstrucción bronquial difusa es en sí
normal, porque la membrana alvéolo capilar no está
alterada como para obstaculizar el paso de los gases. Sin
embargo, si hay enfisema se observa una disminución de
la capacidad de transferencia de gases debida a la reducción
del área de membrana .
La hipoxemia debida a disminución
de la relación /Q
puede corregirse con el ejercicio en los casos leves o medianos
por efecto de la mayor ventilación. Si la alteración
es muy marcada, el ejercicio aumenta la perfusión más
que la ventilación y exagera la hipoxemia. /Q
puede corregirse con el ejercicio en los casos leves o medianos
por efecto de la mayor ventilación. Si la alteración
es muy marcada, el ejercicio aumenta la perfusión más
que la ventilación y exagera la hipoxemia.
ALTERACIONES FUNCIONALES POR COMPROMISO DEL ESPACIO
ALVEOLAR
CAUSAS DE COMPROMISO DEL COMPARTIMENTO
ALVEOLAR
La participación funcional de los
espacios alveolares en la respiración puede verse alterada
por numerosas condiciones y enfermedades de muy diversa naturaleza.
Si bien son muchas las variantes involucradas, los mecanismos
de compromiso del espacio alveolar pueden reducirse básicamente
a tres:
1.- Ocupación del espacio alveolar.
2.- Atelectasia o colapso alveolar.
3.- Eliminación quirúrgica de
áreas extensas del pulmón.
Es obvio que en algunas de estas lesiones el intersticio vecino
a los alvéolos alterados también se compromete.
Sin embargo, la magnitud de esta participación no alcanza
a modificar la fisonomía del cuadro determinado por la
exclusión alveolar. En consecuencia, debe subentenderse
que al referirnos a las alteraciones del compartimento alveolar
lo hacemos en el sentido de que éste es el predominantemente
comprometido.
La ocupación de los alvéolos
puede deberse a exudados (neumonías), ultrafiltrado capilar
(edema pulmonar), sangre (hemorragia pulmonar), células
neoplásicas (cáncer bronquioloalveolar), etc.
El colapso alveolar o atelectasia puede ser
consecuencia de la reabsorción del aire distal a una obstrucción
bronquial localizada total o deberse a la presencia de lesiones
que ocupen espacio dentro del tórax, ante las cuales el
pulmón disminuye de volumen más por retracción
elástica que por compresión. Las enfermedades asociadas
a este mecanismo son muy diversas: neumotórax, derrame
pleural, masas y quistes pulmonares, segmentos o lóbulos
hiperinsuflados, ascenso diafragmático por ascitis, etc.
También pueden producirse atelectasias por retracción
cicatrizal de áreas de pulmón o por hipoventilación,
en la cual se colapsan alvéolos que presentan insuficiente
expansión inspiratoria, especialmente en las zonas dependientes
del pulmón.
Consecuencias funcionales
La variedad de causas y mecanismos explica
que haya múltiples variantes en las consecuencias funcionales
del compromiso del espacio alveolar. Sin embargo, existen algunos
elementos que en conjunto configuran una imagen relativamente
característica:
Volúmenes pulmonares.
Por tratarse de lesiones que específicamente restringen
el espacio alveolar, es lógico que produzcan reducciones
de los volúmenes pulmonares (Figura14-4). Sin embargo,
como veremos, tales alteraciones no son siempre detectables.
Volumen corriente. La
alteración más frecuente es la disminución
de este volumen, que es compensada por un aumento de la frecuencia
respiratoria, con lo que suele resultar una ventilación
alveolar normal o aumentada. Los mecanismos que explican la reducción
del VC son múltiples, pero el más importante es
la disminución de la distensibilidad pulmonar. Esta determina,
como respuesta compensatoria, que se limite el volumen corriente,
probablemente para disminuir el trabajo elástico.
Capacidad vital. Aunque
la exclusión de espacios alveolares restringe directamente
el volumen disponible para esta maniobra, sólo las lesiones
relativamente extensas producen cambios capaces de sacar a la
CV del amplio rango que tienen los valores teóricos normales
y configurar el patrón espirométrico llamado restrictivo.
Así, un sujeto sano con una CV de un 120%
del valor teórico puede tener una lesión que reduzca
su CV a 80%, manteniéndose ésta aún "dentro
de límites normales". La situación es diferente
si existe una espirometría previa o se usa esta medición
para seguir la evolución de un enfermo. A esta limitación
de sensibilidad diagnóstica de la CV se une su falta de
especificidad, ya que se puede reducir por otros mecanismos y
enfermedades muy diferentes: por aumento del VR en obstrucción
bronquial difusa, por rigidez del parénquima en enfermedades
del intersticio, por fallas neuromusculares, por derrame pleural,
etc.
Volumen residual. Dependiendo
de la enfermedad causal, el VR puede estar normal o disminuido,
pero en general se afecta menos que la CV.
Capacidad pulmonar total. Disminuye
principalmente a expensas de la CV.
Resistencia de la vía aérea.
Los espacios alveolares comprometidos no ventilan significativamente,
de manera que el flujo aéreo se realiza a través
de los bronquios normales del resto del pulmón. En consecuencia,
no hay alteraciones de la resistencia de la vía aérea.
El valor absoluto del VEF1 suele disminuir en proporción
a la reducción de la capacidad vital, debido a que disminuye
la cantidad de aire disponible para ser expulsado en el primer
segundo. La conservación de una relación VEF1/CVF
normal indica este hecho y descarta que el VEF1 haya
disminuido por limitación del flujo espiratorio.
Distensibilidad pulmonar.
En casos de ocupación del espacio alveolar o atelectasias,
el área afectada no participa de los cambios de volumen
pulmonar, motivo por el cual no influye directamente en la distensibilidad.
Sin embargo, aunque el pulmón no afectado tiene una distensibilidad
en sí normal representa sólo una parte del volumen
pulmonar normal, por lo cual el volumen corriente normal significa
una mayor distensión. Debido a la forma de la curva presión/volumen
pulmonar (Figura 14-5).esto exige efectuar un cambio de presión
mayor, para lograrlo. En consecuencia, la distensibilidad pulmonar
efectiva en estos casos puede estar disminuida, lo que aumenta
el trabajo elástico.
Intercambio gaseoso.
La presencia de alteraciones de la relación
 /Q
depende de lo que sucede con la circulación capilar
de los alvéolos comprometidos. Si la perfusión está
mantenida o aumentada, como suele observarse en neumonías,
hay disminución de la relación /Q
depende de lo que sucede con la circulación capilar
de los alvéolos comprometidos. Si la perfusión está
mantenida o aumentada, como suele observarse en neumonías,
hay disminución de la relación  /Q
con efecto cortocircuito. En cambio, si los capilares colapsan
en el mismo grado que los alvéolos, como sucede en
algunas atelectasias y neumotórax, el trastorno /Q
con efecto cortocircuito. En cambio, si los capilares colapsan
en el mismo grado que los alvéolos, como sucede en
algunas atelectasias y neumotórax, el trastorno  /Q
es escaso. En enfermos con exéresis quirúrgica,
la relación /Q
es escaso. En enfermos con exéresis quirúrgica,
la relación  /Q
del pulmón remanente es normal. /Q
del pulmón remanente es normal.
Los gases arteriales
en un paciente en particular dependen básicamente de la
magnitud de los trastornos  /Q
existentes, siendo la diferencia alvéolo-arterial el índice
más sensible. En la mayoría de los casos se observa
hipoxemia con PaCO2 normal o disminuida
por hiperventilación compensatoria. La administración
de O2 tiene poco o ningún efecto sobre la PaO2,
debido a que el oxígeno no llega a los alvéolos
ocupados o colapsados. Excepcionalmente, en trastornos muy extensos
como los producidos por edema pulmonar cardiogénico o de
permeabilidad, puede haber retención de CO2,
generalmente debido a fatiga muscular inspiratoria secundaria
al aumento del trabajo respiratorio y a la hipoxemia. /Q
existentes, siendo la diferencia alvéolo-arterial el índice
más sensible. En la mayoría de los casos se observa
hipoxemia con PaCO2 normal o disminuida
por hiperventilación compensatoria. La administración
de O2 tiene poco o ningún efecto sobre la PaO2,
debido a que el oxígeno no llega a los alvéolos
ocupados o colapsados. Excepcionalmente, en trastornos muy extensos
como los producidos por edema pulmonar cardiogénico o de
permeabilidad, puede haber retención de CO2,
generalmente debido a fatiga muscular inspiratoria secundaria
al aumento del trabajo respiratorio y a la hipoxemia.
ALTERACIONES FUNCIONALES POR COMPROMISO DEL
INTERSTICIO
El intersticio pulmonar forma un tejido continuo,
que envuelve los bronquios y vasos intrapulmonares, rellena los
espacios entre los acinos alveolares y se une al tejido conjuntivo
de la pleura visceral. Está formado por sustancia amorfa,
células, fibras elásticas y colágenas. En
su espesor transcurren capilares y linfáticos. Parte de
las fibras se organizan en tabiques, que separan, en forma no
siempre completa, lobulillos, segmentos y lóbulos pulmonares.
En las paredes alveolares pueden distinguirse dos áreas:
una muy fina, óptima para la hematosis, ya que el epitelio
alveolar y el endotelio capilar contacta íntimamente, y
otra gruesa por interposición de tejido intersticial laxo.
Es en esta última área donde primero se acumula
el líquido cuando se produce edema pulmonar, interfiriendo
escasamente en el intercambio gaseoso.
Causas de compromiso intersticial
Las enfermedades que pueden comprometer predominantemente
el intersticio son muy numerosas )
pero pueden reducirse básicamente a la infiltración
intersticial por líquido (edema), células (inflamatorias
o neoplásicas), o tejido fibroso, con diversos grados de
distorsión de la arquitectura pulmonar. Corrientemente
los componentes mencionados se combinan, determinando diversos
grados de engrosamiento y rigidez. Las alteraciones tienden a
ser difusas, pudiendo ser homogéneas o, más frecuentemente,
presentando focos en diferentes etapas de evolución.
Consecuencias funcionales
Un determinante importante del tipo y grado
de las alteraciones funcionales es el carácter difuso o
extenso que presentan estas enfermedades. Las lesiones localizadas
pueden pasar fácilmente inadvertidas.
Al igual que las enfermedades de los espacios
aéreos, las lesiones intersticiales restringen característicamente
los volúmenes pulmonares, pero en este caso el mecanismo
básico es la disminución de las distensibilidad
pulmonar más o menos difusa.
Volumen corriente. Característicamente,
este volumen tiende a disminuir, siendo compensado por un aumento
de la frecuencia respiratoria, lo que mantiene una ventilación
alveolar normal o aumentada. Esta taquipnea es una adaptación
del organismo a la mayor rigidez pulmonar, ya que en esta forma
se requieren cambios de presión menores para obtener el
volumen corriente y, por lo tanto, se efectúa un menor
trabajo muscular respiratorio.
Capacidad vital. Se
encuentra frecuentemente disminuida por la menor distensibilidad
pulmonar y el aumento de reflejos propioceptivos.
Volumen residual y capacidad pulmonar
total. Suelen estar reducidos en forma paralela a la
CV.
Resistencia de la vía aérea.
Generalmente es normal, aunque en algunas de las enfermedades
del compartimento intersticial pueden producirse fenómenos
obstructivos en los bronquíolos. Sin embargo, por las razones
vistas en el capítulo 2, éstos contribuyen poco
a la resistencia total de la vía aérea y, por lo
tanto, no se reflejan en el VEF1. Este indicador se
modifica sólo en relación a los cambios de CVF,
conservándose normal la relación VEF1/CVF.
Distensibilidad pulmonar. La
disminución de la distensibilidad pulmonar es la alteración
más característica de los procesos intersticiales
difusos, y se debe al aumento intrínseco de la rigidez
del parénquima pulmonar (Figura 14-5).

Figura 14-5. Mecanismos de
disminución de la distensibilidad pulmonar. El gráfico
superior izquierdo representa la curva PV normal, que se muestra
como línea interrumpida en los otros. El área
sombreada representa el cambio de presión necesario para
obtener un determinado volumen corriente. En el engrosamiento
intersticial se observa una disminución de la distensibilidad
específica determinada por el pulmón más
rígido. En condiciones en que existe una disminución
del tejido pulmonar funcionante, tales como relleno alveolar,
resección quirúrgica o atelectasia (no mostrada
en la figura), también existe una disminución
de la distensibilidad efectiva, aunque las propiedades elásticas
del pulmón funcionante sean normales debido a que el
cambio de volumen represente una mayor proporción del
volumen total.
A diferencia de lo que sucede en las enfermedades
del espacio alveolar, tanto la distensibilidad efectiva como la
específica están disminuidas, como corresponde al
aumento de rigidez del parénquima ventilado.
Intercambio gaseoso.
El engrosamiento del intersticio produce dos tipos de alteraciones
que generalmente son inseparables. Por una parte, la disminución
de la distensibilidad local determina que ante un mismo cambio
de presión las zonas comprometidas aumenten menos su volumen,
lo cual determina una disminución local de la ventilación
y, por consiguiente, una caída de la relación  /Q.
Por otra parte, el engrosamiento de la pared puede interferir
con la difusión de gases, especialmente del oxígeno.
Este último tipo de alteración sería comparativamente
de menor importancia. Se produce, en consecuencia, hipoxemia que
puede corregirse al administrar oxígeno. Debido al aumento
de la velocidad de circulación, durante el ejercicio aparece
o se acentúa la hipoxemia . La PaCO2
es frecuentemente baja, por su alta difusibilidad. Se observa
hipercapnia sólo en etapas terminales o cuando se agrega
fatiga muscular respiratoria. /Q.
Por otra parte, el engrosamiento de la pared puede interferir
con la difusión de gases, especialmente del oxígeno.
Este último tipo de alteración sería comparativamente
de menor importancia. Se produce, en consecuencia, hipoxemia que
puede corregirse al administrar oxígeno. Debido al aumento
de la velocidad de circulación, durante el ejercicio aparece
o se acentúa la hipoxemia . La PaCO2
es frecuentemente baja, por su alta difusibilidad. Se observa
hipercapnia sólo en etapas terminales o cuando se agrega
fatiga muscular respiratoria.
La medición de la capacidad de difusión
puede cuantificar la magnitud del trastorno, lo que es útil
en investigación o en el control de una evolución
de la enfermedad intersticial crónica bajo tratamiento.
| La identificación de los patrones
obstructivo y restrictivo es un paso inicial que permite reducir
el número de posibilidades en los respectivos diagnósticos
diferenciales |
|
|
