CAPITULO 29ASPECTOS GENERALES DE LAS NEUMONIAS
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla 29-1 AGENTES CAUSALES DE NEUMONÍAS ADQUIRIDAS EN LA COMUNIDAD |
||||||
|---|---|---|---|---|---|---|
| Extrahospitalarias | Intrahospitalarias | UCI |
||||
| (8 estudios) | (35 estudios) | (14 estudios) | ||||
| AGENTE | N | % | N | % | N | % |
| S. pneumoniae | 890 |
15,7 |
8.922 |
21,7 |
1.333 | 21,8 |
| H. influenzae | 890 |
3,5 |
8.922 |
4,7 |
1.333 | 5,1 |
| Gram negativos | 1.039 |
6,7 |
8.922 |
3,4 |
1.333 | 7,6 |
| S. aureus | 890 |
0,2 |
8.922 |
1,5 |
1.333 | 7,2 |
| M. catarrhalis | 654 |
0,0 |
8.922 |
1,4 |
1.148 | 3,8 |
| M. pneumoniae | 1.039 |
4,3 |
8.922 |
6,8 |
1.333 | 2,1 |
| C. pneumoniae | 803 |
13,6 |
8.922 |
6,9 |
1.148 | 6,6 |
| Legionella spp. | 1.039 |
2,0 |
8.922 |
5,0 |
1.333 | 7,2 |
| Influenza A y B | 1.039 |
6,7 |
8.922 |
6,5 |
1.333 | 2,7 |
| Otros virus | 1.039 |
11,9 |
8.922 |
9,4 |
1.333 | 4,8 |
| Mixta | 1.039 |
6,1 |
8.922 |
8,2 |
1.333 | 5,1 |
| Otros | 1.039 |
1,9 |
8.922 |
3,0 |
1.333 | 7,9 |
| Desconocida | 1.039 |
51,3 |
8.922 |
45,7 |
1.333 | 41,8 |
La buena respuesta a agentes betalactámicos
que se observa en la mayoría de los enfermos en los
que no se llega a diagnóstico etiológico sugiere
que la mayor parte de esos enfermos tienen neumonías
neumocócicas o por anaerobios.
Otros microorganismos, como S. aureus, bacilos gramnegativos
entéricos y Legionella spp., causan neumonías
extrahospitalarias con menor frecuencia. No obstante, durante
las epidemias de influenza A, las neumonías estafilocócicas
aumentan su incidencia, debido al aumento de la afinidad de
las células epiteliales por este microorganismo. Las
neumonías por gramnegativos son relativamente más
frecuentes en algunos grupos, como ancianos, pacientes con
enfermedades que comprometen su estado general, diabéticos
y alcohólicos. Por estas razones, se recomienda diferenciar,
dentro del grupo de pacientes con neumonías adquiridas
en la comunidad, a los pacientes internados en casas de reposo
geriátricas o de enfermos crónicos, ya que se
comportan de manera similar a las neumonías nosocomiales.
El resto de los agentes capaces de producir neumonía son menos frecuentes y suelen presentarse en pacientes con factores de riesgo especiales. En los enfermos con enfermedad pulmonar obstructiva crónica (EPOC), por ejemplo, son relativamente más frecuentes las neumonías por Haemophilus influenzae, Moraxella catarrhalis y, en menor medida, los bacilos gramnegativos. En los enfermos con diabetes mellitus, insuficiencia hepática y renal, alcohólicos y ancianos son relativamente más frecuentes los gramnegativos y estafilococo. Por otra parte, en las epidemias de influenza aumenta la frecuencia de las neumonías estafilocócicas.
Si bien existen diferencias clínicas entre los grupos de neumonías causadas por los diferentes agentes, en la práctica las excepciones son demasiado numerosas para que estas diferencias puedan ser útiles en la toma de decisiones terapéuticas individuales. En general, las neumonías por S. aureus y bacilos gramnegativos tienden a ser más graves, con mayor compromiso hemodinámico. Sin embargo, una neumonía neumocócica bacterémica puede ser tan grave como aquéllas, como lo demuestra su letalidad, que, a pesar de tratamiento adecuado alcanza a un 30% en algunas series. Por otra parte, algunas neumonías por Klebsiella spp. y por estafilococos pueden tomar un curso subagudo, con poca gravedad clínica.
Además, es necesario tener presente que hasta en un 10% de los casos pueden
coexistir dos agentes causales, lo que no debe extrañar
si se considera que la infección se produce por aspiración
de secreciones respiratorias altas.
La neumonía del adulto adquirida en la comunidad se manifiesta bajo múltiples
formas que incluyen una o más de las siguientes características:
cuadro agudo de compromiso del estado general, fiebre, calofríos,
tos, expectoración mucopurulenta, dolor torácico
y dificultad respiratoria de magnitud variable. En el examen
físico se comprueba taquicardia, taquipnea, fiebre
y signos focales en el examen pulmonar (matidez, broncofonía,
respiración soplante, crepitaciones).
El diagnóstico clínico de neumonía sin
confirmación radiográfica carece, en general,
de precisión ya que la historia y examen físico
no permiten diferenciar con certeza otras afecciones respiratorias
agudas (infecciones de la vía aérea superior,
bronquitis, influenza). El diagnóstico de neumonía
es clínico-radiográfico: la historia y examen
físico permiten sospechar que existe una infección
pulmonar, pero el diagnóstico se establece con seguridad
cuando se demuestra la presencia de infiltrados pulmonares
de aparición reciente en la radiografía de tórax.
Las diferentes formas de presentación de las neumonías
no guardan una relación específica con los diferentes
gérmenes causales.
Colaboran al diagnóstico en casos dudoso la leucocitosis y desviación
a izquierda en el hemograma y la elevación de proteína
C reactiva ( PCR en castellano y RPC en ingles), como indicadores
proceso inflamatorio.
La radiografía de tórax permite confirmar el
diagnóstico clínico, establecer su localización,
extensión y gravedad; además permite diferenciar
la neumonía de otras patologías con las cuales
se puede confundir, detectar posibles complicaciones, y puede
ser útil en el seguimiento de los pacientes de alto
riesgo. La resolución de los infiltrados radiográficos
a menudo ocurre varias semanas o meses después de la
mejoría clínica, especialmente en el anciano,
en los casos con infección bacterémica, en neumonía
multilobar y en neumonía grave manejada en la UCI.
Aun cuando las manifestaciones clínicas de los enfermos con neumonía son muy variables, hasta hace pocos años se distinguía dos patrones basados en el cuadro clínico-radiográfico: las neumonías clásicas o típicas ocasionadas por S. pneumoniae y otras bacterias, y las neumonías atípicas causadas por Mycoplasma spp. y los virus respiratorios. Se pensaba que el cuadro clínico de la neumonía típica era ocasionado por patógenos respiratorios clásicos como Streptococcus pneumoniae o Haemophilus influenzae, y se describía como caracterizado por síntomas respiratorios agudos, tales como compromiso del estado general, tos, expectoración purulenta o hemoptoica, fiebre, calofríos, dolor torácico, y signos de condensación en el examen pulmonar, asociado a leucocitosis y desviación izquierda en el hemograma, y un foco de condensación lobular en la radiografía de tórax. Se esperaba que la radiografía de tórax mostrara signos de relleno alveolar con diferentes patrones, tales como condensaciones homogéneas o no homogéneas, segmentarias o no segmentarias, foco único o focos múltiples, excavados o no, con o sin cambios de volumen del pulmón afectado, con o sin derrame pleural. Sin embargo. el cuadro clínico descrito se observa sólo en parte de los enfermos, existiendo marcadas variaciones interindividuales que se alejan bastante del cuadro clásico. En los ancianos, por ejemplo, el comienzo puede ser insidioso, con pocos síntomas de localización respiratoria y nula o escasa fiebre y leucocitosis, predominando los síntomas generales, compromiso de conciencia, incontinencia esfinteriana y descompensación de enfermedades crónicas, todo lo cual puede conducir a retraso en la consulta o en el diagnóstico de la neumonía, con un retardo en el inicio del tratamiento antibiótico, lo que seguramente influye en el mal pronóstico que tienen las neumonías en este grupo de edad.
Por otra parte, se calificaba como neumonías atípicas las producidas por otros gérmenes como Mycoplasma pneumoniae, Chlamydia pneumoniae y virus respiratorios, que se manifestaban por síntomas respiratorios de evolución subaguda, con compromiso leve a moderado del estado general, confundible con un síndrome gripal, refiriendo sensación febril de escasa intensidad, tos intensa y persistente, seca o con escasa expectoración mucosa. En general, se consideraban como excluyentes de neumonía atípica los calofríos intensos, el dolor pleural, los signos evidentes de condensación, la leucocitosis mayor de 15.000/mm3 o leucopenia menor de 4.000/mm3. La radiografía característica era la que mostraba lesiones más extensas que las sugeridas por el examen físico y consistía en una mezcla de compromiso intersticial con condensación alveolar, generalmente en pequeños focos múltiples, bilaterales, aunque podían existir focos de condensación segmentarios.
Si bien estas formas de presentación pueden asociarse con mayor frecuencia a algunos agentes causales, no son lo suficientemente específicas, por lo que nunca deben ser empleadas como único criterio para decidir el manejo de un paciente.
Clásicamente se distinguen tres tipos de neumonías según sus características morfológicas en la radiografía:
a) Neumonías alveolares. Se caracterizan por comprometer una zona relativamente
extensa del pulmón, cuyos espacios aéreos o
alvéolos están rellenos con exudado inflamatorio.
La infección se origina en el parénquima pulmonar
y se disemina por los poros de Kohn, por lo que no respeta
límites segmentarios.
b) Bronconeumonías. Consisten en focos de inflamación
que se inician en las vías aéreas y comprometen
los alvéolos que de ellas dependen. Por esta razón
su distribución suele ser segmentaria con múltiples
focos pequeños de condensación.
c) Neumonías intersticiales. El fenómeno inflamatorio
afecta predominantemente el compartimento intersticial, generalmente
en forma difusa, con escasos focos de exudado intraalveolar.
Según estas características morfológicas, las neumonías pueden producir diferentes síntomas y signos en el examen físico y radiografía, elementos que en un tiempo fueron considerados útiles para sospechar el agente causal y orientar el tratamiento. Sin embargo, como ya se ha dicho, estudios más profundos han demostrado que la historia, examen físico y radiografía de tórax no permiten identificar con seguridad el agente etiológico de la infección pulmonar, ya que existe mucha superposición entre las manifestaciones clínicas y radiográficas determinadas por los distintos gérmenes.
Al igual que lo que sucede con los síntomas y signos del examen físico, tampoco existen patrones radiográficos específicos de un germen en particular. El aumento de volumen del lóbulo afectado por una neumonía fue mucho tiempo considerado propio de las neumonías por Klebsiella spp. (Figura 29-3). Sin embargo, se ha demostrado que este signo radiográfico puede ocurrir en cualquier neumonía grave. El infrecuente patrón de nódulos pulmonares múltiples (Figura 30-1), secundario a una siembra hematógena, es sugerente de estafilococo, pero también puede verse en otros microorganismos que se diseminan por esta vía. Por otra parte, la presencia de excavación es poco frecuente en las neumonías neumocócicas y por Mycoplasma spp., por lo que su presencia sugiere más bien estafilococo, anaerobios y gramnegativos. El patrón radiográfico de la neumonía por Mycoplasma puede ser fácilmente confundido con una bronconeumonía bacteriana. Aunque el patrón intersticial es más frecuente en las neumonías virales y las fases iniciales de la neumonía por micoplasma, la presencia de condensación no excluye estas etiologías.
De lo expuesto se deduce que no existe un cuadro típico de neumonía y en consecuencia se confirma que no se justifica la denominación de neumonías atípicas, que se acuñó cuando se describieron los primeros casos de neumonías por micoplasma, clamidias y otros gérmenes. Sin embargo la designación aun se sigue usando ampliamente.
Los espacios aéreos se encuentran llenos de exudado inflamatorio, inicialmente constituido por edema y fibrina al que, posteriormente, se agregan eritrocitos (fase de hepatización roja), que son después reemplazados por leucocitos (fase de hepatización gris). La lesión se inicia en un foco periférico que se extiende centrífugamente por los poros de Kohn, sin respetar límites segmentarios. Esta conducta podría tener relación con una incapacidad de los mecanismos defensivos para detener la diseminación del microorganismo, ya que se observa preferentemente en la infección por gérmenes capsulados (S. pneumoniae, Klebsiella spp.), capaces de resistir la fagocitosis. La imagen radiográfica en estos casos corresponde a una condensación homogénea que puede comprometer todo un lóbulo o, si no lo hace, no tiene distribución segmentaria (Figura 29-2).
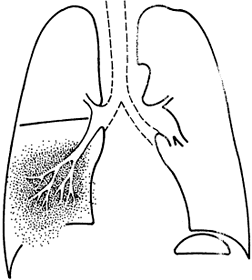
Figura 29-2. Condensación homogénea no segmentaria con broncograma aéreo ubicada en el lóbulo inferior derecho. En caso de neumonías extensas, la condensación puede detenerse en una cisura, como sucede en las figuras 22-11 y 29-3.
Debido a que las vías aéreas están generalmente permeables y rodeadas de tejido pulmonar condensado, se contrastan y se hacen visibles en la radiografía de tórax, constituyendo un broncograma aéreo. En el examen físico suele determinar el clásico síndrome de condensación pulmonar con aumento de la transmisión de la voz y vibraciones vocales, matidez, broncofonía, respiración soplante o soplo tubario y abolición del murmullo pulmonar. Estos signos pueden faltar si el foco de condensación es pequeño o alejado de la pared torácica.
En los pacientes con enfisema, el aspecto radiográfico de este tipo de neumonía cambia, ya que los espacios aéreos de mayor tamaño no se llenan completamente con el exudado inflamatorio, lo que produce una imagen radiográfica de condensación no homogénea. Este tipo de lesión se observa con mayor frecuencia en hombres fumadores mayores de 40 años, los que pueden no haber desarrollado aún síntomas atribuibles a su enfisema pulmonar.
El volumen del pulmón afectado es generalmente normal, pero puede estar levemente aumentado en casos de neumonías muy exudativas, como las producidas por Klebsiella spp. o S. pneumoniae (Figura 29-3).

Figura 29-3. Condensación lobular con aumento de volumen, evidenciado por abombamiento de la cisura horizontal. Este fenómeno puede observarse en neumonías muy exudativas causadas por Klebsiella pneumoniae y, con menor frecuencia, por S. pneumoniae y otros gérmenes.
Ocasionalmente puede observarse una leve disminución de volumen. Si ésta
es marcada, se debe pensar en lesiones obstructivas del bronquio,
especialmente neoplásicas.
Generalmente existen desde el comienzo múltiples focos de inflamación
que se ubican en las vías aéreas finas y desde
allí el fenómeno inflamatorio se extiende a
los alvéolos tributarios. La imagen radiográfica
corresponde a condensaciones pequeñas en focos múltiples
(Figura 29-4).

Figura 29-4. Condensación en pequeños focos bronconeumónicos múltiples, que afectan principalmente los lóbulos inferiores.
Cuando la condensación es más extensa, ella puede adoptar una forma segmentaria, es decir la de una lesión triangular con su vértice dirigido hacia el hilio pulmonar (Figura 29-5).
. 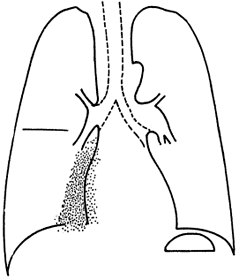
Figura 29-5. Condensación homogénea segmentaria. Se observa en bronconeumonías en las que la condensación se extiende a partir de la vía aérea donde se inicia la inflamación. Generalmente no hay broncograma aéreo. Otras lesiones segmentarias, como la embolia pulmonar, pueden causar una imagen semejante. Se puede saber que la lesión está ubicada en el lóbulo inferior y no en el medio, porque no hay borramiento de la silueta cardíaca.
En estos casos habitualmente no existe broncograma aéreo, ya que la vía aérea se encuentra llena con exudado inflamatorio. Cuando la bronconeumonía es muy extensa, sus focos pueden confluir, produciendo una condensación no homogénea.
Tanto las neumonías alveolares como las bronconeumonías pueden evolucionar hacia la excavación, la que suele adoptar la forma de una cavidad dentro de una condensación . Si está parcialmente llena con líquido se observa un nivel hidroaéreo en su interior. (Figura 29-6).

Figura 29-6. Absceso pulmonar. Se observa una condensación relativamente homogénea del lóbulo superior izquierdo con una cavidad en su espesor, la que presenta un nivel hidroaéreo.
En las neumonía necrotizantes,ocasionadas principalmente por gérmenes
gramnegativos, S. aureus y anaerobios,. pueden verse
múltiples pequeñas cavidades con o sin liquido
evidente.
En su mayoría son causadas por virus y se caracterizan porque el infiltrado inflamatorio se ubica preferentemente en el espesor de los tabiques alveolares, sin comprometer los espacios aéreos. Generalmente afectan en forma difusa ambos pulmones, produciendo una imagen radiográfica de tipo reticular o retículo-nodular. Las lesiones tienden a ubicarse preferentemente en las zonas peribroncovasculares e hiliares. A diferencia de las neumonías alveolares y de las bronconeumonías, en las intersticiales rara vez se produce excavación o derrame pleural importante. (Figura 29-7).

Figura 29.7. Neumonía intersticial con focos intersticiales en los lóbulos inferior derecho, inferior izquierdo y superior izquierdo. Este patrón se observa en neumonías por Mycoplasma y Chlamydia spp.
Los hechos descritos permiten explicar los hallazgos usuales del examen físico. En las neumonías alveolares suele haber un síndrome de condensación pulmonar con aumento de las vibraciones vocales, matidez, aumento de la transmisión de la voz y respiración soplante, además de crepitaciones. En cambio, en las bronconeumonías y neumonías intersticiales no hay signos de condensación pulmonar evidentes y sólo se auscultan crepitaciones en las zonas afectadas. Es necesario tener presente que la sensibilidad del examen físico pulmonar en las neumonías es limitado, ya que hasta en un 50% de los casos las manifestaciones clínicas son incompletas o están ausentes. Por lo tanto, son los signos generales, como fiebre, compromiso del estado general y aumento de la frecuencia respiratoria, junto a los hechos anamnésticos y a la búsqueda sistemática del origen respiratorio en los cuadros infecciosos, los que permiten plantear la neumonía como hipótesis diagnóstica para ser confirmada con un examen radiográfico.
El principal problema para el diagnóstico etiológico de las neumonías es el hecho de que los microorganismos patógenos que causan la mayoría de las infecciones respiratorias suelen estar presentes en las vías aéreas superiores en sujetos sin neumonía, ya sea porque son parte de la flora normal o por colonización. En consecuencia, para atribuir un rol patógeno a un microorganismo determinado es imprescindible tener la seguridad de que la muestra proviene del foco pulmonar, que no se ha contaminado en su paso por las vías aéreas y que ha sido procesada adecuadamente. Si el microorganismo aislado es alguno que nunca forma parte de la flora normal o de colonización el hallazgo es, en cambio, siempre significativo. Dentro de este grupo, el principal ejemplo es el bacilo de Koch, como se verá en el capítulo respectivo. El cultivo de otros microorganismos que son siempre patógenos, tales como virus, Chlamydia spp., Mycoplasma spp., y Legionella spp. se utiliza limitadamente en clínica debido a su elevado costo y complejidad.
Las principales razones para realizar estudios microbiológicos en pacientes con neumonía serían las siguientes:
a) La identificación del agente causal de la neumonía y su patrón
de susceptibilidad a los antimicrobianos permite la selección
de un esquema antibiótico específico.
b) El tratamiento antimicrobiano dirigido, de espectro reducido,
reduce los costos, el peligro de la resistencia antibiótica
y el riesgo de reacciones adversas.
c) Los estudios microbiológicos permiten vigilar el
espectro de patógenos que producen neumonía
a lo largo del tiempo, lo que proporciona valiosa información
epidemiológica sobre las tendencias en los agentes
causales y la resistencia antibiótica en una determinada
área geográfica.
Las dos primeras razones se superan en la mayoría de los casos recurriendo a los tratamientos empíricos establecidos para los 4 grupos en que se pueden diferenciar las neumonías adquiridas en la comunidad que se verán en detalle en el capítulo 64. En cambio, la identificación de gérmenes por interés epidemiológico que se aborda a través de métodos de investigación sigue siendo un argumento válido para hacer exámenes ya sus resultados son indispensables para diseñar tratamientos antibióticos empíricos adecuados.
En clínica, la necesidad de hacer el esfuerzo de identificar el germen causal generalmente sólo se se plantea en neumonías graves o con factores de riego personal o epidemiológico que normalmente requieren participación de especialistas, de manera que el clínico general no necesita dominar el manejo detallado de los exámenes que se verán a continuación, pero sí debe conocer su existencia y potencialidad. Hacen excepción el examen de expectoración y el hemocultivo, cuyo campo de aplicación es más extenso.
Por la rapidez con que los pacientes pueden agravarse, ningún estudio diagnóstico justifica un retraso en el inicio del tratamiento antibiótico más allá de unas pocas horas. En consecuencia, si no es posible tomar una muestra o efectuar una radiografía rápidamente, es preferible comenzar el tratamiento sin mayores estudios.
Es necesario tener presente que un tratamiento antibiótico previo disminuye acentuadamente la sensibilidad y la especificidad de la mayoría de los exámenes microbiológicos de expectoración, sangre y líquido pleural, impidiendo identificar el agente causal y facilitando el aislamiento de gérmenes no relacionados con la neumonía. En consecuencia, estos exámenes no son útiles en pacientes que hayan recibido una o más dosis de antibióticos. Además, el tratamiento antibiótico previo es también capaz de negativizar la mayor parte de las muestras obtenidas por métodos invasivos. De lo anteriormente expuesto se puede concluir que inmediatamente después de hacer el diagnóstico de neumonía es necesario decidir si es necesario y factible un estudio etiológico: si se decide hacerlo se debe proceder a obtener las muestras rápidamente, para iniciar el tratamiento antibiótico sin tardanza. Los estudios deben estar guiados por la gravedad de la neumonía, los factores de riesgo epidemiológico y la respuesta al tratamiento empírico.
En general, no se recomienda realizar exámenes microbiológicos de rutina en el ámbito ambulatorio en los pacientes sin factores de riesgo. Son excepción los pacientes con tos y expectoración persistente y compromiso del estado general, en los cuales debe obtenerse muestras de expectoración para baciloscopias y cultivo de Koch. En los enfermos que son hospitalizados por neumonía comunitaria, su gravedad y riesgo de muerte justifica la realización de exámenes microbiológicos básicos (tinción de Gram y cultivo de expectoración, hemocultivos, cultivo de líquido pleural), intentando pesquisar el agente causal de la infección pulmonar para orientar el tratamiento antimicrobiano específico.
Expectoración. El examen microbiológico de expectoración bien efectuado permite identificar al agente causal en aproximadamente la mitad de las neumonías neumocócicas, en la mayoría de las neumonías por gram negativos y S. aureus y en un número difícil de precisar de neumonías por H. influenzae y Moraxella catarrhalis. El aislamiento de otros agentes patógenos como anaerobios y algunos hongos carece de significado, ya que éstos son habitantes normales de la boca.
Para que un resultado sea significativo se deben cumplir las siguientes condiciones:
a) La muestra debe provenir del territorio alveolar y no ser simplemente saliva
o secreción faríngea. La identificación
de muestras adecuadas se efectúa mediante un examen
citológico al demostrarse la presencia de más
de 25 leucocitos polimorfonucleares y menos de 10 células
epiteliales por cada campo de 100x. El hallazgo de numerosas
células epiteliales bucofaríngeas sugiere que
la muestra está contaminada. Por estas razones es conveniente
asegurarse, antes de iniciar el tratamiento, que las muestras
respiratorias obtenidas son las adecuadas, con el propósito
de obtener un nuevo espécimen si el primero no fue
satisfactorio.
b) El examen debe ser procesado lo antes posible, debido a
que los agentes causales más frecuentes, como S.
pneumoniae y H. influenzae, son muy sensibles a
las condiciones físicas ambientales, por lo que pueden
morir, mientras que otros microorganismos, como S. aureus
y los bacilos gramnegativos, son capaces de sobrevivir
e incluso multiplicarse in vitro. Por estas razones,
las muestras procesadas después de dos horas carecen
de valor.
c) El paciente no debe haber recibido tratamiento antibiótico
antes de tomar la muestra, ya que basta una dosis para que
las bacterias más frecuentes, S. pneumoniae y
H. influenzae, no puedan ser cultivadas. Aun más,
en casos de neumonías neumocócicas o por H.
influenzae es posible cultivar otros gérmenes resistentes
al antibiótico en uso, como estafilococo y bacilos
gramnegativos, que no están jugando ningún rol
patógeno, lo que puede inducir a errores en el tratamiento.
El uso previo de antibióticos también disminuye
la sensibilidad y especificidad del cultivo de expectoración.
El rendimiento diagnóstico y la utilidad clínica del examen dependen de varios factores:
a) La interpretación del examen requiere un experto entrenado.
b) La toma de la muestra requiere un protocolo estricto.
c) El retraso en el transporte y procesamiento de las muestras
afecta su rendimiento.
d) La interpretación del examen es entorpecida por
la contaminación con la microbiota de la cavidad oral.
e) La correlación entre la tinción de Gram y
los cultivos es dependiente de los factores anteriores.
La sensibilidad y especificidad del examen en el diagnóstico de la neumonía neumocócica varía notablemente en diferentes escenarios clínicos, ya que depende críticamente del operador, del estricto cumplimiento de las normas técnicas y criterios de informe.La tinción de Gram es capaz de identificar a los neumococos, con bastante certeza, por su aspecto de cocáceas grampositivas lanceoladas, en pares o cadenas cortas. Con tinciones especiales es también posible observar su cápsula característica. En suma, la presencia de gran cantidad de diplococos grampositivos lanceolados en una muestra de expectoración adecuada (menos de 10 células epiteliales y > 25 leucocitos por campo) sugiere una neumonía neumocócica. Los estafilococos se pueden sospechar por su aspecto de cocáceas grampositivas, generalmente abundantes, ya sea aisladas o en racimos. Las cepas de Haemophilus spp. tienen también un aspecto relativamente distintivo con la tinción de Gram, ya que aparecen como bacilos gramnegativos cortos. El resto de los gramnegativos son también fáciles de detectar, porque usualmente son muy abundantes. Las cepas de Moraxella catarrhalis tienen un aspecto distintivo de cocáceas gramnegativas pequeñas. En general, para que el hallazgo de un germen en la tinción de Gram y el cultivo de esputo pueda considerarse significativo, es necesario que exista concordancia en el o los microorganismos identificados en ambos métodos y que el número sea importante. Si bien se han efectuado estudios con recuentos cuantitativos en expectoración con buenos resultados, su utilidad clínica es dudosa, ya que no difieren mucho de los obtenidos con el análisis semicuantitativo corriente, siempre que éste sea bien hecho.
Expectoración inducida. En algunos enfermos que no expectoran espontáneamente, es posible obtener muestras adecuadas si se efectúa una nebulización con solución hipertónica de NaCl y kinesiterapia respiratoria con tos asistida.
Aspiración traqueal. En pacientes que no expectoran se pueden obtener muestras de secreciones respiratorias aspirando la tráquea con un catéter apropiado. Dado que este tipo de muestra también está contaminada, pues el catéter debe pasar por boca o nariz, su interpretación es similar a la de expectoración. En individuos intubados se puede aspirar directamente la tráquea, pero estas muestras también tienen una contaminación significativa, ya que se ha observado que a las pocas horas de intubación la vía aérea presenta colonización importante por gérmenes potencialmente patógenos, especialmente S. aureus y bacilos gramnegativos. Por este motivo, el aislamiento de pequeñas cantidades de estos gérmenes no tiene un significado necesariamente causal en neumonías de enfermos con vía aérea artificial, pero el análisis cuantitativo del cultivo con recuento mayor de 106 ufc/ml (unidades formadoras de colonias), tiene peso para establecer el diagnóstico de neumonía nosocomial.
Hemocultivo. Los principales agentes bacterianos que se asocian con bacteriemia son S. pneumoniae, H. influenzae, S. aureus y K. pneumoniae. Aun cuando la sensibilidad de los hemocultivos en neumonías por gérmenes aeróbicos es sólo de un 10 -20%, siempre deben obtenerse en enfermos hospitalizados, puesto que , por su especificidad, permiten efectuar un diagnóstico de certeza en pacientes de alto riesgo, ya que la bacteriemia se asocia a un aumento de la letalidad por neumonías de aproximadamente tres veces. En las neumonías por anaerobios, en cambio, la frecuencia de bacteriemias detectables por hemocultivo es de sólo un 3%, razón por la cual no se justifica obtener hemocultivos anaeróbicos en forma rutinaria. El rendimiento de los hemocultivos en la neumonía comunitaria de manejo ambulatorio es inferior al 5%. Por lo tanto, lo recomendable es practicar dos hemocultivos, antes de iniciar el tratamiento antibiótico, en los pacientes graves ingresados al hospital y en los pacientes que no responden al tratamiento empírico inicial.
Líquido pleural. El derrame pleural paraneumónico es la acumulación de líquido pleural exudativo asociado con infección pulmonar ipsilateral (neumonías, absceso pulmonar o bronquiectasias infectadas).Aproximadamente un tercio de los pacientes hospitalizados con neumonía desarrollan un derrame. En la mayoría el líquido es un exudado estéril, ya que se produce por difusión hacia la pleura de mediadores de la inflamación desde el foco neumónico. . La invasión del líquido pleural por microorganismos es siempre una complicación grave e implica la necesidad perentoria de vaciamiento. Por esta razón, la investigación bacteriológica y la búsqueda de signos indirectos de invasión del líquido pleural (pH menor de 7,1, lactato mayor de 5 mmol/L, glucosa baja y LDH elevada) debe hacerse sistemáticamente en todos los pacientes que tengan un derrame paraneumónico de volumen significativo, tanto para detectar precozmente la invasión bacteriana como para obtener un diagnóstico etiológico. A diferencia de los hemocultivos, en el líquido pleural es necesario efectuar cultivos aeróbicos y anaeróbicos, puesto que este último tipo de microorganismos está implicado en aproximadamente un tercio de los casos. Los principales gérmenes aislados en el líquido pleural son bacilos gramnegativos, S. aureus, S. pneumoniae y anaerobios.
Serología. Las pruebas comúnmente usadas detectan anticuerpos séricos (clases igG e igM) frente a Mycoplasma pneumoniae, Chlamydia pneumoniae, virus respiratorios y Legionella pneumophila. En general, sólo se debieran procesar muestras pareadas (fase aguda y convalecencia), a menos que la enfermedad tenga más de una semana de evolución al momento del ingreso.
IgG sérica. Dado que casi todos estos exámenes se modifican sólo después de 2-3 semanas, su utilidad para el manejo del caso individual es escasa. Niveles basales elevados por sobre los encontrados en una población sana permiten hacer un diagnóstico presuntivo retrospectivo. En infecciones por Mycoplasma spp., Chlamydia spp., virus y Legionella spp. se puede efectuar el diagnóstico etiológico demostrando un aumento significativo de los títulos de anticuerpos. En infecciones por hongos también puede ser significativo demostrar cambios en los títulos de IgG. No obstante, su sensibilidad es baja ya que la respuesta inmunitaria en los enfermos susceptibles a neumonías por hongos es generalmente deficiente.
IgM sérica. Dada la corta persistencia de estos anticuerpos, es posible hacer un diagnóstico con aceptable grado de sensibilidad y especificidad durante la fase aguda, pero como el costo de estos exámenes es bastante elevado, su accesibilidad y utilidad en la práctica clínica es relativamente limitada. Se recomienda obtener muestras pareadas para serología en todos los pacientes con neumonía comunitaria grave admitidos a la Unidad de Cuidados Intensivos, en aquellos que no responden a agentes betalactámicos y en pacientes seleccionados con factores de riesgo epidemiológico específicos.
Detección de antígenos. Se han diseñado múltiples técnicas de detección de antígenos de patógenos respiratorios en muestras de expectoración, sangre u orina, con sensibilidad y especificidad variables, que permiten identificar el agente causal de la infección pulmonar.
En general, se recomienda solicitar exámenes de detección antigénica de S. pneumoniae y Legionella pneumophila a los pacientes con neumonía comunitaria grave y en aquellos con fracaso del tratamiento antibiótico empírico. La detección de antígenos de virus Influenza A y B se recomienda en adultos con neumonía que requieren ser hospitalizados y en ancianos durante la época de alta incidencia de influenza.
La reacción de polimerasa en cadena (PCR sigla en inglés) es una técnica de amplificación de ácidos nucleicos que usa secuencias específicas de DNA como marcadores de la presencia de organismos en expectoración, sangre u otras muestras biológicas. La técnica es, en la mayoría de los casos, sensible y, dependiendo del tipo de muestra, muy específica. Además, los resultados de PCR no están influenciados por el tratamiento antibiótico previo. La sensibilidad extrema de la PCR es una de sus principales limitaciones. El ensayo puede contaminarse con material exógeno y puede ser difícil diferenciar infección activa de colonización cuando se practica PCR en secreciones respiratorias. Las pruebas de PCR se han utilizado para detectar infecciones respiratorias por M. pneumoniae, C. pneumoniae, L. pneumophila y virus, demostrando tener mayor sensibilidad que el cultivo. Se han empleado en la evaluación de pacientes inmunocomprometidos con neumonía adquirida en la comunidad y neumonía nosocomial, pero aún no han tenido gran impacto en las decisiones clínicas y morbimortalidad asociadas a la infección pulmonar.
La escasa sensibilidad de los exámenes no invasivos y la falta de especificidad de los exámenes de expectoración han llevado al diseño de procedimientos invasivos para obtener muestras respiratorias poco contaminadas. El uso de este tipo de exámenes es controvertido, ya que la mayoría de los pacientes con neumonías por germen desconocido mejoran si son tratados con esquemas empíricos racionales. No obstante, en algunos pacientes es necesario obtener este tipo de muestras, ya que el ensayo a ciegas de diversos esquemas puede implicar excesiva demora en aplicar un tratamiento óptimo, costo económico demasiado alto o un riesgo de toxicidad inaceptable:
a) Pacientes inmunodeprimidos, en los que el número de probables microorganismos causales es muy numeroso.
b) Pacientes con fracaso de tratamiento antibiótico, en los cuales puede ser necesario identificar con certeza el germen causal y conocer su sensibilidad.
c) Pacientes con neumonías graves y elevado riesgo de complicaciones, en los cuales un eventual fracaso del tratamiento empírico implique un riesgo de muerte elevado.
d) Cuando los medicamentos empleados en el tratamiento tienen un riesgo elevado, como ocurre, por ejemplo con la Anfotericina B en neumonías supuestamente causadas por hongos.
e) Cuando existe la posibilidad de que se trate de neumopatías no infecciosas, tales como neoplasias, neumonitis por drogas, neumonitis por hipersensibilidad, etcétera.
La selección de estos métodos debe discutirse con especialistas y depende de la disponibilidad local, de las condiciones del enfermo y de los microorganismos probables. La fibrobroncoscopia con catéter telescopado y cepillo protegido, el lavado broncoalveolar con o sin protección, la aspiración transtraqueal y la aspiración pulmonar con aguja fina son técnicas que permiten obtener muestras de las vías aéreas inferiores con escasa o nula contaminación con la microbiota orofaríngea. Las dos últimas se encuentran, en la práctica, abandonadas por los riesgos implícitos en el procedimiento y porque requieren de operadores expertos para su ejecución. En cambio, la tinción de Gram y cultivo de cepillo protegido y lavado broncoalveolar han demostrado buena sensibilidad y especificidad en la identificación del agente causal de las neumonías en diferentes contextos clínicos. .
Los exámenes invasivos más utilizados en
la práctica clínica son:
Biopsia pulmonar por toracoscopía. Es la muestra con mayor sensibilidad y especificidad, pero por su invasividad se reserva para pacientes inmunodeprimidos graves en quienes la identificación precisa del germen causal se considere crucial.
Esta denominación tiene el defecto de sugerir que sería el hospital en sí mismo el único determinante de la neumonía, lo que no es efectivo desde el momento en que sólo una minoría de los pacientes internados la contraen y que el personal que allí trabaja no la presenta en absoluto. Si bien en el hospital es donde existe el riesgo de exposición a los gérmenes causales son, en general, las condiciones del paciente o los procedimientos que estas exigen, las que facilitan el contagio. Esto no exime al hospital de su obligación de implementar las medidas que eliminen al máximo los gérmenes del ambiente, instrumental y equipos y establecer los protocolos que impidan el traspaso de microbios entre enfermos (aislamiento , lavado de manos médicos, estudiantes, personal, etc.)
La neumonía intrahospitalaria (NAH) es la segunda infección nosocomial en frecuencia y la más frecuente en las unidades de cuidados intensivos (UCI). Para estos efectos se considera que una neumonía ha sido adquirida en el hospital o cuando se hace evidente 48 a 72 horas o más después del ingreso, ya que si se presenta antes de este plazo se presume que estaba desarrollándose previamente a la hospitalización del paciente. La neumonía adquirida en la Unidad de Cuidados Intensivos por el paciente conectado a ventilador mecánico es una subclase de neumonía nosocomial neumonía asociada a ventilador (NAV), que se asocia a elevada morbimortalidad, prolonga la estadía en el hospital e incrementa significativamente los costos de la atención. Las neumonías adquiridas en centros geriátricos o de enfermos crónicos son en gran medida similares a las NAH. El problema de los enfermos con alteraciones inmunitarias graves se aborda más adelante
Las neumonías se producen por la deficiencia de los mecanismos defensivos para eliminar los microorganismos que llegan al territorio alveolar, generalmente por aspiración de secreciones de las vías aéreas altas colonizadas por agentes patógenos. La colonización por flora normal (Streptococcus spp., Staphylococcus spp. y Haemophilus spp.) o patógenos adquiridos en el hospital (bacilos gramnegativos entéricos o S. aureus resistente a la meticilina) precede al desarrollo de la neumonía. En los pacientes hospitalizados, especialmente en los más graves, existen múltiples condiciones que favorecen la colonización por patógenos, su llegada al pulmón, y alteraciones de sus mecanismos defensivos que entorpecen la eliminación de los microorganismos que alcanzan el territorio alveolar (Tabla 29 - 2).
|
TABLA
29-2 CONDICIONES ASOCIADAS A NEUMONIAS NOSOCOMIALES |
|
| Favorecen aspiración | Alteración
de conciencia Trastornos de deglución Anestesia - Sedantes |
| Instrumentación respiratoria | Terapia inhalatoria Intubación Traqueostomía Ventilación mecánica |
| Alteración de la flora | Antibióticos Antiácidos bloqueadores H2 de la bomba de protones |
| Alteración de los mecanismos defensa generales | Cáncer Neutropenia Desnutrición Heridas de la piel Quemaduras Corticoides Antineoplásicos Diabetes mellitus Edad avanzada Enfermedades crónicas |
| Alteración de la tos y mecanismos defensivos locales | Cirugía
abdominal alta Cirugía torácica Heridas Quemaduras Vías venosas Intubación Sonda nasogástrica |
Mecanismos secundarios son la inhalación de aerosoles (infecciones por virus respiratorios, Legionella spp. o M. tuberculosis), la siembra hematógena de catéteres intravasculares infectados, la translocación bacteriana del tracto gastrointestinal y la diseminación desde estructuras contiguas.
Las condiciones enumeradas determinan que los microorganismos que causan NAH sean diferentes de los causales de infección extrahospitalaria y que su gravedad sea mucho mayor. Como consecuencia de los trastornos relacionados a la enfermedad de base o de su tratamiento, cerca de un 60% de los pacientes tienen colonización de sus vías aéreas superiores, principalmente por bacterias gram negativas y estafilococo. Muchos de estos microorganismos, especialmente en el medio hospitalario, son resistentes a los antimicrobianos, lo que dificulta aun más su tratamiento. Por todas estas razones las NAH tienen muy mal pronóstico, con letalidades que fluctúan entre 30 y 50%.
Debido a que la colonización se produce generalmente en el hospital, los microorganismos causales son variables según las áreas geográficas, e incluso en diferentes instituciones y servicios. Los patógenos respiratorios involucrados varían según las características de la población examinada, la enfermedad de base, el tiempo de exposición al riesgo y el lugar de ingreso (tipo de hospital, UCI médica, quirúrgica o coronaria). Debido a los mecanismos descritos tienden a ser polimicrobianas. Los agentes más frecuentes en las neumonías nosocomiales son los bacilos gramnegativos, entre los cuales sobresalen Klebsiella pneumoniae, por su gran frecuencia, así como algunos gérmenes resistentes a la mayoría de los antibióticos, tales como Pseudomonas aeruginosa y Acinetobacter calcoaceticus. Cualquier otra bacteria gramnegativa puede causar NAH.
El Staphylococcus aureus es un microorganismo que también se observa con alta frecuencia, destacando su mayor incidencia en diabéticos, en pacientes politraumatizados o con vía aérea artificial, o con vías venosas, así como su transmisión por personal portador. A diferencia de la infección estafilocócica adquirida en la comunidad, suele ser resistente a meticilina.
Aunque su identificación es difícil, los gérmenes anaerobios, aisladamente o en conjunto con aerobios, son también importantes agentes causales de las neumonías nosocomiales, las que se presentan especialmente en aquellos con mayor riesgo de broncoaspiración, por enfermedades del SNC, trastornos de deglución o uso de drogas depresoras de SNC, incluida la anestesia general.
Otros microorganismos como S. pneumoniae, H. influenzae, hongos, Legionella y virus son menos frecuentes.
El diagnóstico de la NAH se sustenta en su aparición después de las 48 horas del ingreso, sus manifestaciones clínicas y los hallazgos radiográficos, y se confirma mediante exámenes microbiológicos. Las manifestaciones clínicas determinadas por la enfermedad de base, así como el empleo de fármacos que bloquean la respuesta inflamatoria sistémica, como los corticoides, antiinflamatorios y antineoplásicos, pueden enmascarar la neumonía, ocasionando retraso en su diagnóstico y tratamiento. En estos enfermos, además, son más frecuentes las embolias pulmonares, el edema pulmonar cardiogénico y no cardiogénico y la toxicidad pulmonar por drogas, condiciones que dificultan el diagnóstico diferencial. Por las razones anteriores, es importante tener un alto grado de sospecha para hacer un diagnóstico precoz e iniciar oportunamente el tratamiento.
Las manifestaciones clínico-radiográficas son inespecíficas, por lo que no permiten efectuar un diagnóstico etiológico. No obstante, la presencia de excavación debe hacer plantear con mayor probabilidad algunos agentes, como S. aureus, ciertos gramnegativos, anaerobios y hongos.
El estudio microbiológico de expectoración es difícil de interpretar, ya que por la enfermedad de base suele haber colonización de las vías aéreas superiores por patógenos. No obstante, debido a que es frecuente que las neumonías sean causadas por los mismos microorganismos que colonizan las vías aéreas altas, a falta de otras muestras, el examen de expectoración o aspirado traqueal cuantitativo suelen ser usados como guía de tratamiento. Sin embargo, debe tenerse presente que son frecuentes las discrepancias entre los microorganismos cultivados en la expectoración o aspirado traqueal y el agente causal de la neumonía determinado por hemocultivos o por muestras no contaminadas. Por este motivo, si no se identifica el agente causal por un método confiable, es preferible cubrir empíricamente los gérmenes más probables, incluyendo obviamente a los cultivados en las muestras respiratorias.
Siempre deben obtenerse hemocultivos y cultivos de líquido pleural en los que tengan derrame puncionable. Es recomendable obtener baciloscopias de expectoración en los enfermos con neumonías nosocomiales, aun cuando éstas podrían omitirse si la evolución radiográfica demuestra que la aparición de las lesiones fue brusca.
En estos pacientes se suelen emplear métodos más agresivos para obtener muestras que permitan establecer el diagnóstico etiológico, variables en cada institución. Las principales técnicas invasivas empleadas actualmente para la toma de muestras en pacientes hospitalizados que se sospecha NAH son el cepillo protegido (CP) y el lavado broncoalveolar (LBA). El objetivo de las técnicas invasivas es tomar una muestra representativa de la secreción bronquial que se origina en el parénquima pulmonar infectado y que no se encuentre contaminada por flora que coloniza el tracto respiratorio superior. Aunque en casos individuales su aporte puede ser decisivo, su real utilidad en el conjunto de pacientes no está bien determinada.
Por todas las consideraciones anteriores, el manejo diagnóstico de estos enfermos debe ser multidisciplinario, participando el médico tratante, los microbiólogos, infectólogos y los especialistas en enfermedades respiratorias.
A diferencia de las neumonías observadas en pacientes con inmunidad normal o poco alterada, en estos pacientes la lista de posibles agentes causales es muy numerosa. En la Tabla 64 - 6 se puede observar que, además de seguir predominando los germenes corrientes como el neumococo, se agregan microorganismos incapaces de causar infección a individuos con inmunidad normal, por lo que se les denomina oportunistas.
| Tabla
29 - 3 ETIOLOGIA DE LAS NEUMONIAS EN PACIENTES INMUNODEPRIMIDOS |
| Bacterias Hongos |
La complejidad del sistema inmune determina que existan múltiples tipos
de alteraciones en su funcionamiento, que que disminuyen
las defensas ante determinados tipos de microorganismos.
En la Tabla 64 - 7 se muestran algunos trastornos inmunitarios
y los gérmenes asociados con mayor frecuencia a cada
condición.
| Tabla
29-4 MICROORGANISMOS PROBABLES SEGUN TRASTORNO INMUNITARIO |
||
Mecanismo |
Enfermedad o condición |
Microorganismo |
| Disminución de granulocitos | Leucemias Ciclofosfamida y otras drogas |
Staphylocccus aureus Bacilos gramnegativos Apergilluss spp. Candida spp. |
| Disminución
de monocitos, macrofagos, linfocitos T |
Enf. Hodgkin
SIDA Corticoides Ciclosporina Insuficiencia renal |
Pneumocystis
jiroveci Micobacterias Nocardia spp. Candida spp. Virus herpes-CMV |
| Déficit de anticuerpos | Mieloma
múltiple Leucemia linfática aguda y crónica Corticoides Antineoplásicos |
S.pneumoniae Haemophilus spp. P. aeruginosa Bacilos gramnegativos |
Debe tenerse presente que con frecuencia estos mecanismos se suman. Es así como en un linfoma, por ejemplo, en que se afecta inicialmente sólo a la inmunidad celular, se agregan, como consecuencia de la quimioterapia, mecanismos que afectan la inmunidad humoral y la cantidad de granulocitos.
El manejo de las neumonías en pacientes con inmunodepresión grave es extremadamente complejo ya que, por una parte, los microorganismos capaces de producir infección pulmonar son muy numerosos, y por otra el diagnóstico diferencial debe efectuarse con muchas condiciones capaces de simular una neumonía (Tabla 29-4).
| Tabla
29-5 CAUSAS DE INFILTRADOS PULMONARES EN PACIENTES INMUNODEPRIMIDOSOS |
| Infecciosas
Toxicidad por drogas antineoplásicas
Neumonitis actínica
Compromiso neoplásico
Hemorragia pulmonar
Tromboembolismo pulmonar
Atelectasias
Derrame pleural
Edema pulmonar
Síndrome de distrés respiratorio agudo
Enfermedad injerto contra huésped
Neumonitis inespecífica
Neumonía en organización criptogénica
Bronquiolitis obliterante
|
 |