| |
El edema pulmonar es una condición de
alto riesgo que el clínico general debe saber detectar
y según su tipo tratar o derivar al sitio adecuado.
Al igual que en otros tejidos, las condiciones
hemodinámicas del capilar pulmonar determinan que normalmente
exista salida del líquido de los capilares al intersticio.
Éste no se acumula debido a que es removido por los linfáticos,
con lo cual el tejido pulmonar mantiene una cantidad óptima
de fluidos. La acumulación excesiva de líquido en
el pulmón se denomina edema pulmonar, el cual de acuerdo
a la ecuación de Starling puede clasificarse en cuatro
grupos, de los cuales sólo los dos primeros son los de
mayor importancia clínica:
1.-Por aumento de la presión hidrostática
capilar: edema hemodinámico. Este grupo incluye las
causas más frecuentes de edema pulmonar. El mecanismo básico
es una elevación de la presión hidrostática
capilar hasta exceder el efecto protector de la presión
oncótica normal de las proteínas plasmáticas,
lo que habitualmente sucede con presiones mayores a 20-25 mmHg.
Recientemente se ha observado que una hipertensión capilar
pulmonar marcada puede producir también un daño
en la integridad de la barrera alvéolo-capilar, determinando
un aumento simultáneo de la permeabilidad, llamado falla
capilar por stress. No se ha establecido si este fenómeno
tiene alguna trascendencia clínica, pero de ser cierto,
implicaría que el edema hemodinámico y el de permeabilidad
podrían combinarse en ciertas circunstancias. Las causas
de edema hemodinámico son variadas:
Hipervolemia absoluta. Es
el resultado de sobrehidratación, debido a la administración
rápida y excesiva de expansores del plasma o por el acceso
de líquidos de irrigación a un lecho vascular abierto
dentro de una víscera hueca, como puede ocurrir en la prostatectomía.
Elevación de la presión venosa pulmonar. Determina
inevitablemente un aumento de la presión capilar pulmonar
y puede observarse en la insuficiencia cardíaca izquierda,
en las lesiones de la válvula mitral y durante arritmias
de alta frecuencia.
Aumento del flujo sanguíneo pulmonar. Por la distensibilidad
del circuito menor, el aumento de flujo debe ser considerable para
elevar la presión capilar, lo que puede ocurrir ocasionalmente
en ejercicios extremadamente violentos y en cortocircuitos intracardíacos
de izquierda a derecha resultantes de perforaciones del tabique
interventricular por infarto del miocardio o heridas penetrantes
cardíacas.
2.-Por un aumento de la permeabilidad capilar:
edema de permeabilidad. Es el segundo en frecuencia y su mecanismo
es una pérdida de la integridad de la membrana alvéolo-capilar,
permitiendo el libre paso de las proteínas plasmáticas
al intersticio pulmonar. Con ello se aumenta la presión
oncótica en el intersticio facilitando la retención
de líquido en éste.
3.-Disminución de la presión
oncótica de las proteínas plasmáticas.
Aunque la presión oncótica de las proteínas
del plasma es un factor crítico en la mantención
de un adecuado balance de líquidos en el pulmón,
rara vez es la causa primaria de edema pulmonar.
4.-Por obstrucción linfática.
Se desconoce si en seres humanos puede jugar un rol importante
en la génesis del edema pulmonar. En animales, la obstrucción
mecánica de los linfáticos pulmonares produce
edema, aunque generalmente transitorio.
Causas misceláneas. Excepcionalmente,
puede producirse edema por mecanismos no completamente aclarados,
como ocurre durante la expansión rápida de un
pulmón previamente colapsado por un neumotórax
o un derrame pleural. El edema pulmonar de altura suele producirse
al ascender sobre 3000 metros, especialmente en personas no
aclimatadas, y tampoco tiene una causa clara, al igual que el
edema neurogénico causada por hipertensión endocraneana,
aunque en ambos casos parece existir una vasoconstricción
pulmonar intensa, probablemente hipóxica en el primer
caso y debida a una hiperactividad simpática en el segundo
caso.
A continuación analizaremos la patogenia y las manifestaciones
clínico-radiográficas del edema pulmonar, con
énfasis en el cardiogénico. El edema pulmonar
por aumento de permeabilidad o distrés respiratorio del
adulto será abordado en detalle en el capítulo
57.
CONSIDERACIONES MORFOLOGICAS
El líquido de edema puede acumularse
en el intersticio o dentro del alvéolo. Estos dos espacios
forman compartimentos relativamente separados y el líquido
se acumula inicialmente en el intersticio y pasa a los alvéolos
sólo en etapas avanzadas del edema intersticial, debido
a la mayor permeabilidad del endotelio en comparación
con el epitelio alveolar. La unión entre células
endoteliales es relativamente laxa y la de las células
alveolares es mucho más estrecha (Figura 46-1).
Figura 46-1. Morfología
alvéolo-capilar. El diagrama muestra una pared alveolar
situada entre dos espacios aéreos. En la región
alvéolo-capilar existen zonas con intersticio grueso,
donde puede acumularse líquido, y zonas delgadas,
donde el intersticio es prácticamente inexistente
ya que ambas membranas basales se encuentran fusionadas.
En la ampliación se muestra la membrana basal (mb),
la unión estrecha entre dos células epiteliales
y la unión laxa entre células endoteliales.
En un período inicial, el líquido
extravasado se acumula en el intersticio extra-alveolar que
rodea vasos y bronquios, área de tejido laxo donde las
presiones son más negativas que en el intersticio que
está en contacto con los alvéolos. Desde allí
se mueve siguiendo el gradiente de presiones hacia el tejido
intersticial de los hilios, que posee presiones más negativas
aun. Por esta razón, cuando el líquido excede
la capacidad linfática de drenaje, se acumula primero
en las regiones hiliares, formando manguitos alrededor de las
vías aéreas centrales y de los vasos del hilio.
Esto explica por qué la distribución del edema
hemodinámico es preferentemente central, a diferencia
del edema de permeabilidad, en el cual el daño difuso
del epitelio alveolar permite que el líquido extravasado
al nivel capilar pase directamente a los alvéolos.
Cuando la acumulación de líquido
sobrepasa la capacidad de estos reservorios, se produce la entrada
de líquido a los alvéolos, lo que disminuye el
radio de curvatura de la interfase aire-líquido, lo que,
de acuerdo a la ley de Laplace, aumenta la tendencia al colapso
alveolar (Figura 2-14). Por otra parte, una vez iniciado, el
paso de líquido llenan bruscamente el alvéolo,
lo que explica la rapidez con que se puede desencadenar el edema
alveolar. Como la reducción de radio no es igual en todos
los alvéolos, se produce coexistencia de alvéolos
llenos de líquido al lado de otros que aún ventilan.
ETIOPATOGENIA
Las fuerzas que gobiernan el movimiento de
líquidos en el pulmón fueron analizadas previamente
y dependen de la ecuación de Starling y de la eficacia
del sistema linfático. Es conveniente recordar que existen
dos tipos de fuerzas contrapuestas: unas que favorecen la transudación
de fluidos y otras que se oponen a ello, y un sistema de drenaje,
el sistema linfático, que en condiciones patológicas
aumenta considerablemente su flujo.
Las fuerzas que favorecen la salida
de líquido al intersticio son:
• La presión hidrostática
capilar.
• La presión hidrostática
intersticial, que es negativa y actúa, por lo tanto,
“succionando” líquidos desde el compartimento
vascular.
• La presión oncótica intersticial, que
tiene efectos variables. Cuando está aumentada, como
ocurre en el edema de permeabilidad por el libre paso de proteínas
al intersticio, favorece la salida de líquidos desde
el capilar. En cambio, cuando baja al diluirse las proteínas
en el edema hemodinámico reduce la filtración
desde el capilar
Las fuerzas que se oponen a la filtración
de líquidos son:
• La presión oncótica capilar, que tiene
el mismo efecto variable que la presión oncótica
intersticial. Aumenta en el edema hemodinámico, debido
a que la transudación de un líquido libre de proteínas
aumenta su concentración en el plasma, favoreciendo así
la retención de fluidos en el compartimento vascular. Sin
embargo, disminuye en el edema de permeabilidad, por la salida
de proteínas al intersticio, favoreciendo el efecto contrario.
• La presión intersticial cuando es positiva frena
la salida de líquido, fenómeno que ocurriría
en los pacientes conectados a ventilación mecánica.
Aun cuando la distinción conceptual entre edema
hemodinámico y por aumento de la permeabilidad es
muy clara, en clínica ambos tipos se combinan con
frecuencia. Como ya se ha mencionado, en el edema hemodinámico
la permeabilidad puede aumentar la falla capilar por estrés�.
Por otra parte, en muchos casos de edema de permeabilidad
se puede agregar un componente de hipertensión capilar
ligado a la condición causante del edema de permeabilidad:
depresión miocárdica en las sepsis, por sobrehidratación
en el tratamiento del shock o por concomitancia con enfermedad
cardíaca.
EFECTOS FISIOPATOLOGICOS
En la etapa intersticial, el edema estimula los
receptores J, provocando taquipnea e hiperventilación alveolar,
que se traduce en un descenso de la PACO2.
Además disminuye la distensibilidad pulmonar, lo que, junto
a lo anterior, aumenta el trabajo respiratorio provocando disnea.
A esto puede agregarse algún grado de edema bronquial,
con aumento de la resistencia de la vía aérea. En
este período, el intercambio gaseoso no se ve afectado,
pero cuando el edema inunda los alvéolos, se produce hipoxemia
por la presencia de cortocircuitos funcionales.
MANIFESTACIONES CLINICAS
Síntomas y signos
Dependen de la magnitud del edema y varían
según la enfermedad causal. En general, el signo más
precoz es la taquipnea que, a pesar de su inespecificidad, sirve
como signo de alarma en los pacientes con riesgo de edema pulmonar.
Usualmente se agrega disnea y, a veces, tos seca en la fase intersticial
y con expectoración espumosa en la etapa de edema alveolar.
El examen físico puede ser negativo o mostrar abundantes
crepitaciones, auscultándose ocasionalmente sibilancias.
Pueden también agregarse signos de derrame pleural.
Manifestaciones radiográficas
Las alteraciones radiográficas varían
según la etapa del edema. El edema intersticial se manifiesta
por una disminución de la transparencia pulmonar, que puede
ser difícil de evaluar. La acumulación de líquido
alrededor de los vasos pulmonares determina que sus contornos
pierdan la definición que normalmente tienen. La acumulación
de líquido en el tejido intersticial de los tabiques interlobulillares
determina la aparición de líneas de Kerley B (Figura
46-2). Eventualmente, en aquellas vías aéreas atravesadas
longitudinalmente por los rayos, puede observarse el engrosamiento
de la pared bronquial por edema. En casos más marcados,
el edema se acumula en el tejido intersticial subpleural, lo que
puede traducirse en un engrosamiento de las cisuras.
El edema alveolar se manifiesta por sombras de
relleno alveolar, cuya cantidad depende de la magnitud del edema.
Generalmente se observa en manchones, con tendencia a la confluencia
en el tercio medio de los pulmones (Figura 46-2).
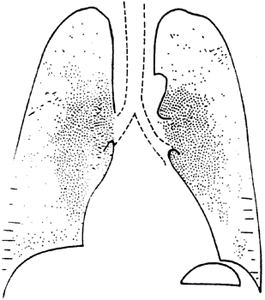
Figura 46-2. Edema pulmonar. El edema del
intersticio se traduce por borramiento de la trama vascular
y presencia de líneas de Kerley. El edema alveolar
da sombras de relleno que se disponen simétricamente
alrededor de los hilios, produciendo una imagen en mariposa.
El aumento de tamaño del corazón indica que
en este caso el edema es cardiogénico.
La distribución del edema varía
considerablemente entre los enfermos dependiendo del mecanismo
causal, pero en los casos de edema hemodinámico característicamente
se sitúa en forma simétrica perihiliar (edema en
mariposa). La forma puede variar según la posición
en que haya estado el paciente por desplazamiento gravitacional
del líquido
Es frecuente observar derrames pleurales uni
o bilaterales, que muestran alguna predilección por los
espacios cisurales donde, al acumularse, pueden dar sombras pseudotumorales
La presencia de una silueta cardíaca aumentada y la redistribución
del flujo sanguíneo sugieren edema cardiogénico.
La rápida regresión de los signos de edema apoya
una etiología hemodinámica, mientras que una regresión
más lenta es propia del edema por permeabilidad.
TRATAMIENTO
El tratamiento debe dirigirse tanto a la enfermedad
causal como a la emergencia pulmonar. Lo más urgente es
combatir la hipoxemia con oxígeno en altas concentraciones.
Si éstas resultan ineficaces, como ocurre si el cortocircuito
es de gran magnitud, debe considerarse el uso de ventilación
mecánica. El principal objetivo de ésta es distender
los alvéolos semicolapsados llenos de líquido, de
manera que éste se disponga como una capa sobre las paredes
del alvéolo distendido, interfiriendo menos en la hematosis,
y posiblemente ayudar a la reentrada del líquido al intersticio,
como consecuencia de la presión positiva intraalveolar.
Además, la ventilación mecánica tiene un
efecto beneficioso sobre la función cardíaca, pues
al generar una presión positiva intratorácica disminuye
el retorno venoso. Un efecto adicional importante es que disminuye
o elimina el trabajo respiratorio, lo que evita la fatiga muscular
respiratoria y reduce el consumo muscular de O2,
lo que trae como consecuencia un incremento en la disponibilidad
miocárdica de O2.
La terapia específica para el edema hemodinámico
corresponde a la de la alteración cardíaca causal.
|
|
